Die Früherkennung von Krebs ist der Schlüssel zur Verbesserung des Patientenüberlebens, doch bestehende Technologien werden durch unzureichende Sensitivität und Spezifität herausgefordert. Viele Methoden basieren auf invasiven Untersuchungen oder weisen eine hohe Falsch-Positiv-Rate auf, was ihre weitverbreitete Anwendung einschränkt. In den letzten Jahren hat die Flüssigbiopsie-Technologie aufgrund ihrer Nicht-Invasivität große Aufmerksamkeit auf sich gezogen, aber auch ihre Einschränkungen bei der gezielten Tiefensequenzierung haben ihre Entwicklung eingeschränkt.
Früherkennung ist bei der Krebsbehandlung immer ein heikles Thema. In den letzten Jahren hat die Flüssigbiopsie-Technologie aufgrund ihrer Nicht-Invasivität und hohen Empfindlichkeit große Aufmerksamkeit erhalten. Bestehende Erkennungstechnologien basieren jedoch meist auf einer gezielten Tiefensequenzierung und lassen sich nur schwer mit mehreren Datentypen integrieren, was Auswirkungen auf die Sensitivität und Spezifität hat.
Als Reaktion auf dieses technische Manko entwickelte ein Forschungsteam der Universität Oxford eine neue multimodale Nachweismethode für zirkulierende Tumor-DNA (ctDNA), die auf der genomweiten TET-unterstützten Pyridin-Boran-Sequenzierung (TAPS) basiert. Das größte Highlight dieser Methode ist, dass sie Genom- und Methylierungsdaten gleichzeitig analysieren kann, wodurch die Sensitivität der Krebsdiagnose 94,9 % und die Spezifität 88,8 % erreicht. Diese bahnbrechende Technologie bietet neue Möglichkeiten für die Krebsfrüherkennung und Patientenstratifizierung.
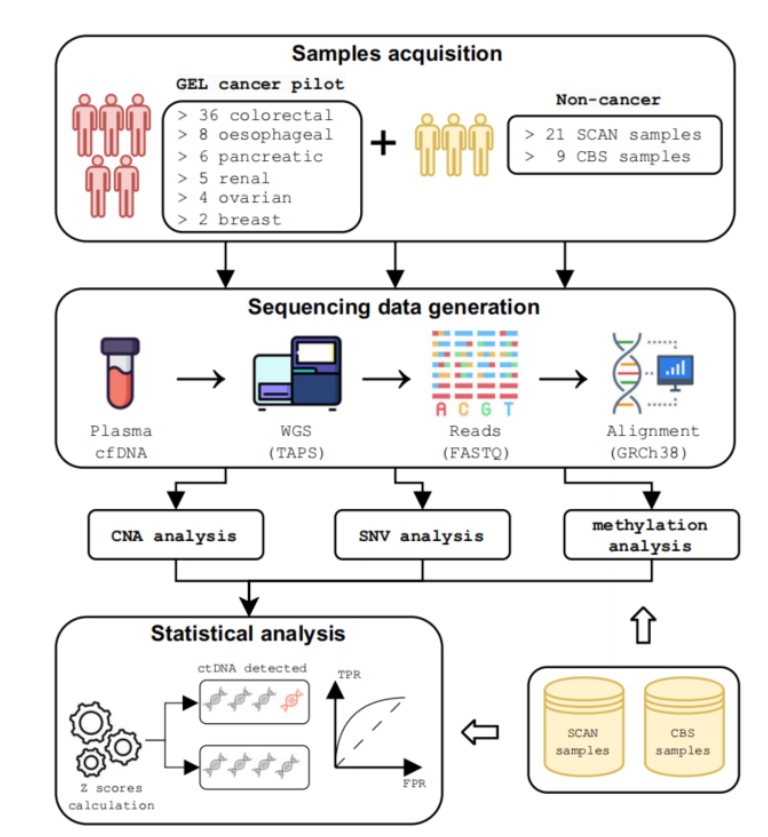
Die Studie mit dem Titel „Multimodale zellfreie DNA-Gesamtgenome-TAPS ist empfindlich und offenbart spezifische Krebssignale“ wurde am 8. Januar 2025 in der Fachzeitschrift „Nature Communications“ veröffentlicht. Der Forschungshintergrund zeigt, dass die Früherkennung von Krebs zwar entscheidend für die Verbesserung der Patientenprognose ist, aktuelle Screening-Methoden jedoch nur weniger als 30 % der Krebsarten abdecken können und viele Methoden invasive Untersuchungen erfordern und eine geringe Akzeptanz haben. Obwohl die Früherkennungstechnologie für mehrere Krebsarten eine nicht-invasive Erkennung ermöglichen kann, ist die Falsch-Positiv-Rate bei asymptomatischen Menschen oft hoch, was ihre Anwendung einschränkt.
Die TAPS-Technologie des Oxford-Teams nutzt eine zerstörungsfreie Methode, um eine hohe Empfindlichkeit bei niedrigem ctDNA-Gehalt aufrechtzuerhalten. Die Forscher überprüften die Genauigkeit dieser Methode bei mehreren Krebsarten durch Tiefensequenzierung von Proben von 61 Krebspatienten und 30 Nicht-Krebs-Kontrollen.
Das Team entwickelte außerdem eine multimodale Datenanalyse-Pipeline, die Variationen der Kopienzahl, somatische Mutationen und Methylierungssignale integriert, um die Empfindlichkeit des ctDNA-Nachweises zu verbessern. Die Ergebnisse zeigten, dass in klinischen Proben die Nachweisempfindlichkeit dieser Methode 85,2 % erreichte, was viel höher war als die Ergebnisse einer einzelnen Datenmodalität.
Obwohl diese Methode erhebliche Vorteile bei der Früherkennung von Krebs und der postoperativen Überwachung gezeigt hat, steht sie in der praktischen Anwendung immer noch vor Herausforderungen, wie z. B. hohen Sequenzierungskosten und ressourcenbeschränkten klinischen Umgebungen. Zukünftige Studien können die Sequenzierungstechnologie weiter optimieren, um ihre Anwendbarkeit auf weitere Krebsarten zu erweitern.
Diese Forschung des Teams der Universität Oxford bringt neue Hoffnung für die Früherkennung von Krebs und ihre hohe Sensitivität und Spezifität bilden eine solide Grundlage für eine präzisere Krebsdiagnose und -behandlung in der Zukunft. Obwohl weiterhin Herausforderungen bestehen, werden Fortschritte in dieser Technologie zweifellos den Bereich der Krebsbehandlung voranbringen und mehr Patienten Vorteile bringen.